杏彩平台官网「品种」就像是母亲,「受理号」是她十月怀胎的孩子,品种第一胎可能生的是个三胞胎,第二胎是个双胞胎,第三胎只有一个宝宝。
第一胎的 3 个是老大,最后离家都去干临床试验了,都有了点成绩,第二胎的 2 个看着不错,也去跟着 3 个老大干临床试验了,结果,老四比 3 个老大干的还好,老五失败了,灰溜溜的跑回家了,因为 3 个老大和老四的帮助,老六特别顺利的走上了上市之路,出名了,干出了一番伟绩。
也就是说,一个药品品种可能有多个受理号,每个受理号,在 CDE(药审中心)、CFDA(总局)的状态又会各不一样。
如果是做投资、做竞品或者是自己产品的数据分析,建议是从品种角度,再细化到每个受理号的状态,最后回归到品种本身,因为这样,更能从整体上说明问题。
看到留言的时候,小编开始冒冷汗了,靠数据吃饭的,数据肯定是没啥问题的,那,是数据处理错了吗?
一般来说,只有完成了临床试验的申报上市的药品,会有临床数据,才会需要进行临床数据自查核查。如果是在申请临床阶段,应该就不需要核查了。
比如奥希替尼,有 14 个受理号,2 个是上市申请外,其余全是临床申请,也就是说在 JXHL1600100申请临床时,因为奥希替尼这个品种之前做过批准过临床,有实验数据,所以需要先核查早前的受理号的临床试验数据的真实性。
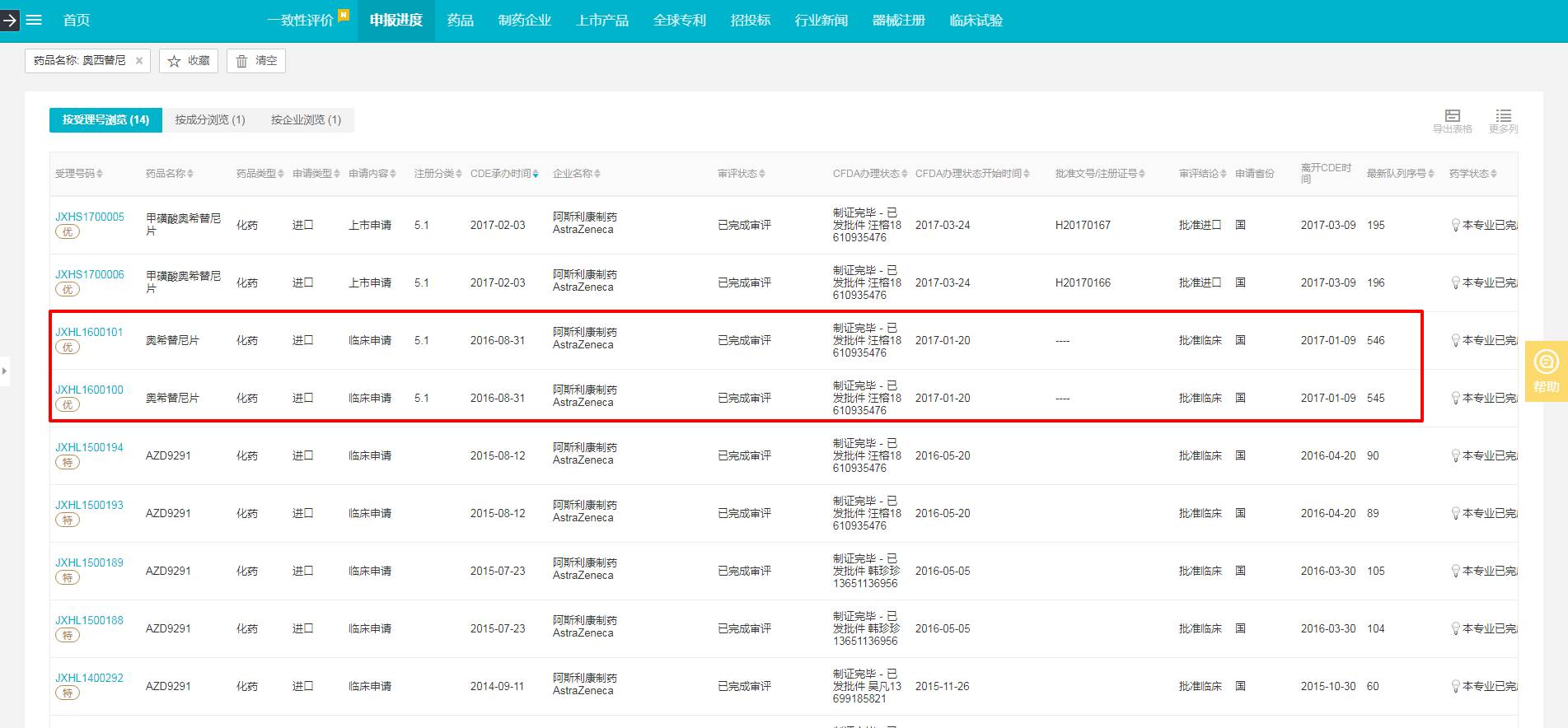
临床申请都还没通过,就需要临床数据核查,这样的情况,勃林格殷格翰制药的尼达尼布、吉利德的来迪派韦索磷布韦也都出现了。
然而奥希替尼杏彩体育,看上去就像是个例外。奥希替尼(受理号 JXHL1600100)11 月纳入优先审评, 12 月底公示现场核查,一个插曲是 2017 年 1 月公示的自查名单中,奥希替尼也赫然在列,不过受理号是 JXHL1600101。
说奥希替尼是先核查在自查,是没错,毕竟本是同根生,但专业一点的说法可能是,奥希替尼尾号为 100 的受理号先核查了,然后尾号为 101 的要求企业自查了。
这里,我们可以看下 BMS 的两个丙肝新药,盐酸达拉他韦片 BMS 报产两个受理号, JXHS1600062和 JXHS1600068,其中 JXHS1600062撤回了,JXHS1600068没有进入临床自查和现场核查,取得了批文,BMS 另一个品种阿舒瑞韦软胶囊的情况也一样。

当然,以上的问题,都是因为小编没有注意到品种和受理号的微妙关系,导致失之毫厘谬以千里,以后在表述上会更加严谨的。
另外,在我们上次发布文章震惊!优先审评品种, 4 天就能完成临床自查核查之后,有一些用户在后台反馈了一些其他的疑惑,感谢 @奶茶 @晨光 @家琦
有一部分信息,可能是企业和国家局的专属信息,没有被公示,这部分信息, Insight 数据库从数据层面无法获取到,所以会出现数据与信息不一致。
比如,吉利德的来迪派韦索磷布韦列入了自查名单,没有纳入到核查计划,但据说,这个品种已经完成了临床核查,和文中提到的跳过核查直接审评审批不相符。
同样,强生(西安杨森)的西美瑞韦,申报临床阶段虽然审的很快,但关联的申报上市阶段是被临床核查给「卡住」了,实际的审评时间应该是超过了 4 天。
还有一种情况是 ,国家局核查都是列特定的受理号,但真正核查的时候,极有可能把该品种所有的受理号全部都核查一遍,但这实际操作,外界无法知道。
小编翻阅政策以及询问资深人士后,发现自己之前的流程图有错误,CDE(负责药品审评)CFDI(负责药品检查)暂时从政策上看是同步的,并没有孰先孰后,「跨过现场核查直接开启审评」一说也不严谨,一般情况下, CFDI 会在核查之后将结果汇总到 CDE,再出审批结论,最后由 CFDA 审批制证。

原因是这样子的,国家局会公示纳入优先审评品种名单表,当一个品种进入到这个列表,就默认为正式纳入优先审评,这个时间也会算作是正式纳入优先审评,显示到 Insight 数据库时光轴上。

但这个正式纳入优先审评时间,国家局并没有公示,现在公示在列表中的时间,是该品种拟纳入优先审评的时间,参考意义不大。

按理说,应该采用数据库里体现的正式纳入的时间,但这次为了数据出处有迹可循,我们使用的是药审中心表单中的公示时间。
最后,感谢大家对上一篇文章的关注,再次感谢@奶茶 @晨光 @家琦,非常专业的指出我们问题,小编将为 3 位送上丁香园文化衫作为谢礼,麻烦 3 位看到后,在后台回复下地址-姓名-联系方式,小编收到后,会立马送出。(完)
想看更细致的分析企业品种,点击点文末的「阅读原文」!免费升级权限,支持「受理号」和「品种」翻转分析。

访问手机版

微信公众号